Blitzzusammenfassung_ (in 30 Sekunden)
- Organtransplantationen retten seit den 1960ern, als das Problem der Abstoßungsreaktion angegangen werden konnte, regelmäßig Leben.
- Ein großes Problem ist der Mangel an Spenderorganen.
- Lösungsvorschläge – von Widerspruchslösungen bis zu Organhandel – sind entweder nur marginal wirksam oder ethisch kompliziert.
- Eine Lösung wäre die Xenotransplantation: die Nutzung tierischer Organe.
- Sie wird seit dem frühen 20. Jahrhundert erprobt, doch erst seit 2020 häufen sich Erfolge.
- Genetisch modifizierte Schweineorgane haben Erfolge erzielt – und derzeit leben zwei Menschen mit funktionierenden Schweinenieren, einer seit rund 8 Monaten.
- Ein Technologieführer steht nun vor einer Studie mit 33 Patienten. Sie könnte wegweisend werden.
- Damit eröffnen sich ethische Fragen, vor allem rund um das Tierwohl und das Risiko einer Verbreitung tierischer Krankheitserreger.
Der Pfad der Technologie_
(4 Minuten Lesezeit)
Ein Stück Geschichte wurde im Jahr 1883 geschrieben: Die erste gesichert gelungene Transplantation der Menschheitsgeschichte war erfolgt. Der spätere Schweizer Nobelpreisträger Theodor Kocher transplantierte Schilddrüsengewebe in einen Mann, welchem er zuvor die Schilddrüse komplett entnommen hatte. Es war die erste sogenannte allogene Transplantation (Allotransplantation) der Welt: Spender und Empfänger waren nicht genetisch verwandt, gehörten aber immerhin derselben Art an.
Transplantationen vor der Moderne
Kulturell existierte das Konzept der Transplantation bereits seit der Antike, auch wenn die Glaubwürdigkeit der überlieferten Geschichten nicht überbewertet werden sollte. Dass der chinesische Gelehrte Bian Que im 3. Jahrhundert v. Chr. die Herzen eines Mannes mit starkem Geist, doch schwachem Willen, und eines Mannes mit schwachem Geist, doch starkem Willen transplantierte, dürfte eher metaphorisch verstanden werden. Und dass die römisch-arabischen Heiligen Damian und Cosmas im 3. Jahrhundert n. Chr. ein ganzes Bein transplantierten, ist ebenfalls unwahrscheinlich.
Etwas realistischer ist, dass der indische Chirurg Sushruta im 2. Jahrhundert v. Chr. eine Hauttransplantation vornahm, auch wenn der Erfolg der Prozedur unklar ist. Noch älter – und der früheste berichtete Eingriff überhaupt – ist eine auf dem 3.500 Jahre alten ägyptischen Ebers-Papyrus überlieferte Hauttransplantation. Bestätigt ist, dass der Italiener Gaspare Tagliacozzi im 16. Jahrhundert erfolgreich eine solche plastische Chirurgie leistete. Der Vorteil dieser Chirurgen war, dass es sich bei den Hauttransplantationen um sogenannte autogene Transplantationen (Autotransplantationen) handelte: Spender und Empfänger waren dieselbe Person, eine Abstoßreaktion des Körpers findet nicht statt.
Die erste Welle
Mit Theodor Kochers Durchbruch 1883 begann eine rasante Phase an wissenschaftlicher Begeisterung. Erst experimentell an Tieren wie Hunden und Gazellen, später an Menschen. Arterien, Venen, Augenhornhaut und Hoden wurden in dieser Zeit transplantiert, mit wechselnden Erfolgen. Ein Vorreiter war der Franzose Alexis Carrel, welcher für seine Arbeit den Nobelpreis erhielt. Er spielte auch eine Rolle dabei, das Prinzip der Abstoßung zu verstehen: Das Immunsystem des Empfängers erkennt transplantiertes Gewebe als Fremdkörper und attackiert es.
Die Abstoßungsreaktion blieb über Jahrzehnte das Hauptproblem der Transplantation und machte es vorerst unmöglich, größere, überlebenswichtige Organe wie Nieren und Herzen zu transplantieren. Eine Ausnahme waren identische Zwillinge: Eine solche syngene Transplantation hat keine Abstoßung zu befürchten. Also gelang 1954 in den USA die erste längerfristig erfolgreiche Nierentransplantation zwischen Zwillingen. Der Empfänger lebte noch 8 Jahre lang. 1959 gelang eine Nierentransplantation zwischen nichtidentischen Zwillingen, wo das Abstoßungsrisiko ebenfalls verringert ist – doch erstmals relevant wurde.
Der allogene Durchbruch
In den 1960ern konzentrierte sich das noch immer exotische Feld auf die Suche nach immunsuppressiven Therapien, also Mitteln, die Abwehrreaktion des Körpers zu unterdrücken. In Tierversuchen wurden erste passable Mittel gefunden, und kurz darauf begann eine zweite Welle an Meilensteinen: 1962 gelang die erste allogene Nierentransplantation, also zwischen zwei nicht verwandten Individuen – und das erste Mal, dass das Organ von einem toten Spender stammte. Kurz darauf folgten die ersten Transplantationen von Herzen, Lebern, Bauchspeicheldrüsen, Lungen, Gebärmuttern und weiteren Organen, später auch von ganzen Händen und Gesichtern.
Der Durchbruch in der Allotransplantation war auch wichtig, weil mit ihr der Kreis der potenziellen Spender regelrecht explodierte. Es waren nicht nur identische Zwillinge, sondern theoretisch konnte fast jeder zum Organspender und eben auch zum Organempfänger werden – insofern die gesundheitliche Verfassung die höchst invasive Prozedur erlaubte. Und insofern Blutgruppe und Gewebemerkmale von Spender und Empfänger kompatibel sind, um die Abwehrreaktion des Körpers zu mildern.
Gut zu wissen: Bei Nieren und Lebern können Transplantationen dank neuer Behandlungsformen auch möglich sein, wenn die Blutgruppe nicht übereinstimmt. Noch beliebter sind als Lösung jedoch "Crossover"-Transplantationen: Hat ein freiwilliges (und selbstverständlich lebendes) Spender-Empfänger-Paar nicht die richtigen Voraussetzungen, wird es mit einem anderen Paar mit demselben Problem gematcht. Die Paare spenden bzw. empfangen praktisch "über Kreuz".
Der Organmangel
Mit der Realisierung allogener Transplantationen bekam die Technologie die Chance, die medizinische Realität für viele Menschen zu ändern und selbst unheilbare Krankheiten zu kurieren. Nun geriet jedoch das Angebot zum Flaschenhals. Das Global Observatory on Donation and Transplantation (GODT) zählte 2023 über 172.000 Eingriffe, was jedoch nur rund 10 Prozent der globalen Nachfrage abdeckte. Vor allem Nierenspenden werden benötigt.
In den USA gab es 2024 rund 24.000 Transplantationen. Davon fast drei Viertel von verstorbenen Spendern, der Rest als Lebendtransplantation. Auf der Warteliste der Empfänger stehen derweil fast 107.000 Menschen. In Deutschland gab es 2024 3.013 transplantierte Organe von 953 Organspendern (rund 200 der Organe stammten aus dem Ausland), doch am Ende des Jahres blieben 8.575 Menschen auf der Warteliste. Auf jede Person auf der Warteliste (welche zudem nicht jene Menschen umfasst, die nicht mehr transplantierfähig sind) kommen also 0,1 Spender bzw. 0,35 Organspenden.
Die Debatte_
(4 Minuten Lesezeit)
Religion und Verteilung
Die Transplantation von Organen ist ein ethisch viel diskutiertes Konzept, denn sie berührt die Idee einer "Vollständigkeit" des Menschen und Unversehrtheit seines Körpers. Im Judentum, Christentum und Islam gab es anfangs kontroverse Debatten über die Praxis, bevor sie (abseits konservativerer Fraktionen) weitestgehend akzeptiert wurde. Eine große Frage war die Definition des Todes, also etwa, ob die Feststellung eines Gehirntods genügt, um Organe entnehmen zu dürfen.
Eine andere große Frage schließt an das Angebots- und Verteilungsproblem an. Erst einmal der Verteilungsaspekt: Wie wird entschieden, wer ein rares Organ erhält und in welcher Reihenfolge? Das könnten Ärzte tun, doch in der europäischen Warteliste Eurotransplant, welcher Deutschland und sieben andere Länder angehören, tut es ein System nach vorab festgelegten Kriterien: die medizinische Dringlichkeit und die Erfolgsaussichten, etwa mit Bezug auf die Verfassung des Patienten und das Risiko einer Abstoßungsreaktion.
Die Verteilungsfrage hat eine Fairnessdimension. Ärmere Länder mit schwächeren Gesundheitssystemen haben weniger Kapazitäten zur Organspende. Menschen dort haben damit weniger Zugang zu lebensrettenden Transplantationen als in reicheren Ländern, und das persönliche Einkommensniveau kann stark über den Zugang zu Spenderorganen entscheiden. Letzteres gilt auch in reicheren Ländern mit nicht allzu egalitären Gesundheitssystemen: Reichere US-Amerikaner können zwar nicht (offiziell) auf Wartelisten vorrücken, doch wissen sie überhaupt, dass sie sich auf mehreren Listen gleichzeitig eintragen können – und sind imstande, entsprechend zu reisen. Das erhöht ihre Überlebenswahrscheinlichkeit messbar, wie Studien bestätigen.
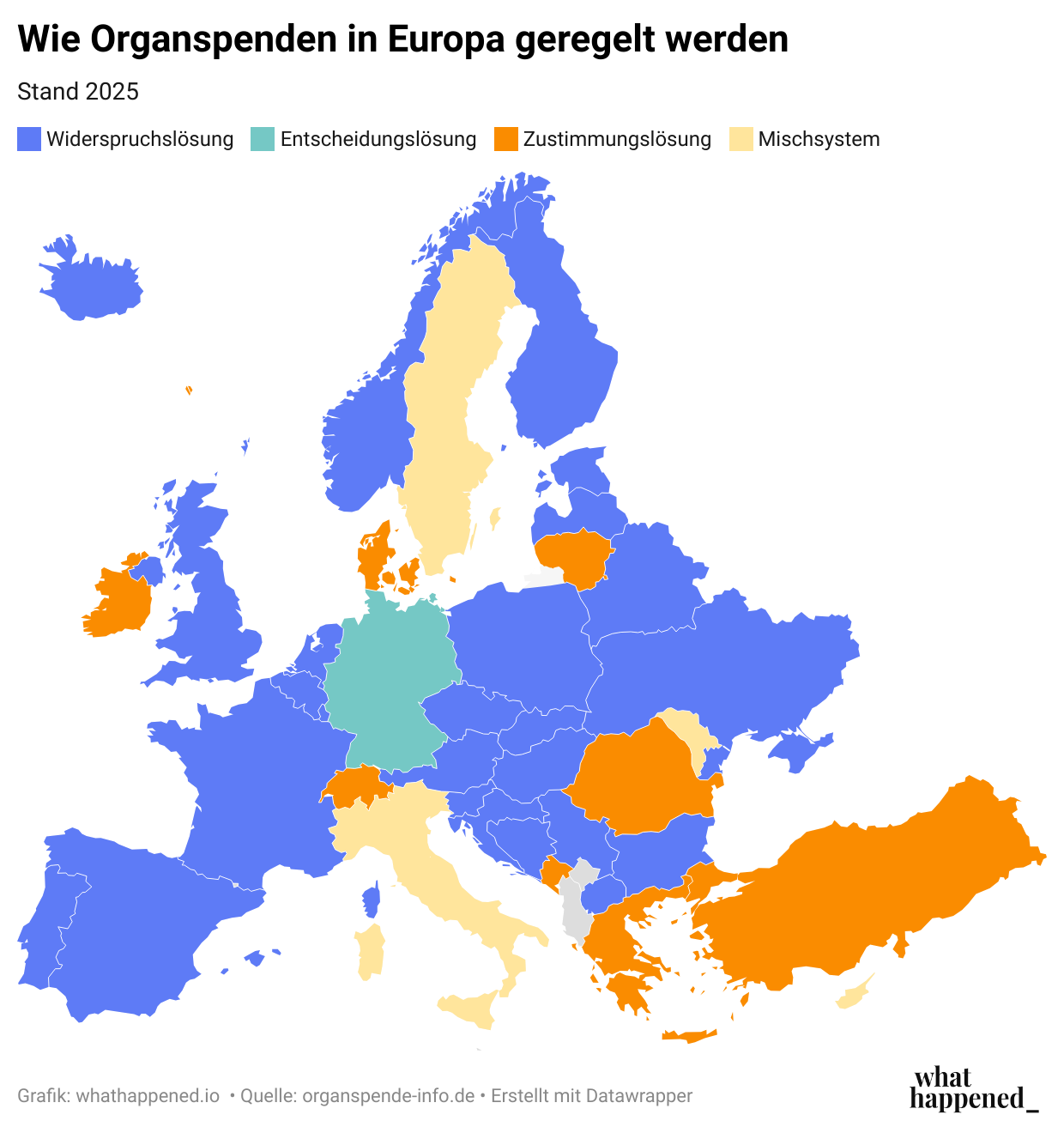
Widerspruchs- vs. Zustimmungslösung
Dann die Angebotsproblematik. Wenn es an Organen mangelt, könnten sie verstorbenen Menschen ohne deren Zustimmung entnommen werden – doch das wird überwiegend abgelehnt; die Souveränität des Verstorbenen wird also höher als der medizinische Vorteil des Erkrankten gewichtet.
Weniger extrem, doch noch immer kontrovers, ist der Vorschlag, die Organspende zumindest zur Grundannahme zu machen: Eine Widerspruchslösung würde jeden Menschen zum Organspender machen, insofern er nicht ausdrücklich widerspricht. Sie existiert z.B. in den meisten Ländern Europas. Ein anderes Modell ist die Zustimmungslösung: Nur, wer ausdrücklich zugestimmt hat, darf nach dem Ableben für die Spende genutzt werden.
Gut zu wissen: Die Widerspruchslösung erhöht zwar den potenziellen Spenderkreis deutlich, führt laut mehreren Studien aber nicht zu tatsächlich mehr Organspenden. Ein Grund scheint zu sein, dass zwar die Zahl der verstorbenen Spender steigt, jene der lebenden Spender sinkt. Forscher sehen die Widerspruchslösung bzw. Varianten davon somit eher als ein Puzzlestück in einem Maßnahmenmix zur Steigerung der Spenderzahlen, nicht aber als Rundumlösung.
Das deutsche Modell
Deutschland setzt seit einer Gesetzesänderung 2022 auf die "Entscheidungslösung". Sie ist im Grunde eine erweiterte Zustimmungslösung: Liegt keine Entscheidung des Verstorbenen vor, werden die Angehörigen befragt und können zugunsten einer Organspende entscheiden. Außerdem sollen Bürger bei der Entscheidung unterstützt werden, indem sie von den Ausweisstellen von Bund und Ländern regelmäßig mit Aufklärungsmaterial und Organspendeausweisen ausgestattet werden. Die Änderung hat die Zahl der Spender tatsächlich etwas gesteigert, aber nur um knapp 10 Prozent und auf Niveaus, welche bereits 2018 erreicht worden waren.
Organhandel
Wenn es an Organen mangelt, wie wäre es, sie auf dem freien Markt verfügbar zu machen? Die ethischen Probleme damit sind groß genug, dass der Organhandel weltweit verboten ist – mit dem Iran als einziger Ausnahme (in Indien war er bis 1994, auf den Philippinen bis 2008 gestattet). Die ethische Dimension ist komplex: Sollten Erwachsene die Möglichkeit haben, ihren eigenen Körper für monetären Nutzen einzusetzen, ähnlich wie bei der Frage über Prostitution?
Die Probleme sind beachtlich. Organhandel bevorteilt erneut wohlhabendere Menschen und wirft damit Fairnessfragen auf; er droht mit irreparablen Schäden für ärmere Menschen, welche vermutlich aus Notlagen handeln; und er birgt das Risiko, dass Menschen die Entscheidung aufgrund von Druck von außen, persönlichen Notlagen oder krimineller Aktivität nicht wirklich selbstbestimmt treffen. Der Profitanreiz hinter Organverkäufen könnte Qualitätsmangel und somit Gesundheitsrisiken für alle Parteien kreieren, wenn Anbieter bei Vorabprüfungen und Sicherheitsstandards einsparen, wie es vor allem in Ländern mit schwächeren Institutionen ein Risiko wäre.
Der Schwarzmarkt
Da ein legaler Organhandel nicht existiert (und auch im Iran nur zwischen iranischen Staatsbürgern gestattet ist), floriert stattdessen ein Schwarzmarkt mit Organen. Wie groß er ist, ist jedoch unklar. Die WHO schätzte 2005 "konservativ", dass 5 Prozent aller transplantierten Organe illegal gekauft worden waren. Jüngere Schätzungen, darunter vom GODT, belaufen sich eher auf 10 Prozent. Manche Forscher kamen im Verlaufe der Jahre auf deutlich höhere Zahlen – doch in der Natur des Schwarzmarkts liegt, dass er schwierig einzuschätzen bleibt. Der Anreiz für den illegalen Organhandel ist derweil intuitiv: Es ist ein Weg, die Warteliste mit ihrem großen Nachfrageüberschuss zu umgehen.
Es gibt also ein großes Angebotsproblem bei Organen, und Lösungsideen sind wahlweise ethisch umstritten oder nur marginal wirksam. Vielleicht kommt die Rettung... durch das Schwein.
Xenotransplantation_
(6 Minuten Lesezeit)

Frühe Versuche
Wenn menschliche Organe rar sind, können tierische Organe als Ersatz herhalten? Erste Versuche mit der sogenannten Xenotransplantation gab es bereits in der aktiven experimentellen Phase des frühen 20. Jahrhunderts. 1905 wurde einem Kind eine Hasenniere transplantiert, 1906 gab es Versuche mit Schweinen und Ziegen und 1923 mit einem Lamm. Alle Versuche scheiterten und die Patienten starben, auch wenn die allerersten Stunden und Tage mitunter vielversprechend aussahen.
Die erste ernstzunehmende Xenotransplantation fand 1964 statt, also inmitten der "zweiten Welle" derTransplantationsforschung. Ein interdisziplinäres Team in den USA rund um Dr. Keith Reemtsma setzte sechs Patienten mit schwerem Nierenversagen Organe von Schimpansen ein. Tatsächlich sind die Nieren der Schimpansen in Größe und Funktion vergleichbar und die Bluttypen A und O nützlich. Auch dank der Fortschritte in der Immunsuppression überlebten die Patienten zwischen 11 Tagen und 9 Monaten, was im Feld als Erfolg betrachtet wurde.
Spätere Versuche mit Primaten scheiterten und die anfängliche Begeisterung ließ nach. In den USA, wo die Forschung am weitesten war, senkten erfolgreiche Programme zur Beschaffung von Organen von verstorbenen Patienten die Notwendigkeit für Xenotransplantation. Die Forschung endete jedoch keineswegs vollständig: 1984 wurde einem als "Baby Fae" bekannten Säugling ein Pavianherz eingesetzt. Sie starb 21 Tage später, weil die Blutgruppe des Pavians nicht passte. Die Transplantation sollte von Anfang an nur vorübergehend sein, doch ein passendes menschliches Spenderorgan ließ sich nicht rechtzeitig finden.
Gut zu wissen: Das Präfix "xenos" stammt aus dem Altgriechischen und bedeutet "fremd" oder "Fremder"; es findet sich auch im Begriff Xenophobie, also Angst vor Fremdem. Um frühere griechische Begriffe aus diesem Explainer zu erklären: "Allos" bedeutet "ein anderer". "syngen" ist das griechische "syn" (zusammen) und "genos" (Familie, Art). "Autos" steht wiederum für "selbst".
Das Schwein zur Rettung
Schweine wurden 1997 zum ersten Mal als Spender eingesetzt. Ihre Organe sind in Größe und Funktion noch etwas geeigneter als jene von Primaten; zudem sind sie einfach zu züchten und übertragen vergleichsweise wenige Krankheiten. Reguläre, also nicht genetisch modifizierte Schweineherzen, -lungen und -nieren wurden bei der ersten Transplantation 1997 in Indien in einen 32-jährigen, schwerkranken Patienten eingesetzt. Er starb kurz nach der Operation an mehreren Infektionen – und die beteiligten Ärzte wurden aufgrund von unethischem Verhalten und fahrlässiger Tötung verurteilt.
Lange war das die Realität der Xenotransplantation: Kuriositäten und Grundlagenforschung, welche nur für ethisch uneindeutige Verzweiflungstaten reichte. Das änderte sich in den 2020ern.
Die Gentechnik als Toröffner
Eine Vielzahl an Erfolgen gelang ab 2021, hauptsächlich, weil Fortschritte in der Gentechnik erlaubten, die medizinischen Schwachstellen umgehbar zu machen. Im September 2021 gelang es Ärzten, eine Schweineniere in einen hirntoten Patienten einzusetzen, ohne, dass eine Abstoßreaktion stattfand. Zuvor war das Kohlenhydrat Alpha-gal per Genmodifikation aus der Niere entfernt worden.
Im Januar 2022 wurde ein genetisch modifiziertes Schweineherz in einen todeskranken Patienten transplantiert. Er starb zwei Monate nach der Operation, nicht zwingend aufgrund des Herzens. Im Juni und Juli 2022 gab es zwei weitere Herztransplantationen, allerdings nur aus Forschungszwecken in verstorbene Menschen. Im Juli 2023 erfolgte eine zweite Nierentransplantation, diesmal in einen Verstorbenen. Im September 2023 wurde erneut ein genetisch modifiziertes Schweineherz transplantiert, doch der Patient starb aufgrund einer Abstoßungsreaktion.
Im März und April 2024 wurden erstmals zwei Schweinenieren in lebende Menschen transplantiert. Beim zweiten Fall, mit einer von der Biotechfirma Revivicor modifizierten Niere, musste das Organ nach einigen Wochen herausgenommen werden – was allerdings offenbar mit einem Mix aus gesundheitlichen Problemen zusammenhing, ohne welche die Niere womöglich nicht abgestoßen worden wäre. Der erste Fall war noch erfolgreicher: Die Firma eGenesis des prominenten Genetikers und Harvard-Professors George Church hatte an einer Schweineniere 69 genetische Veränderungen vorgenommen, darunter 7 menschliche Gene hinzugefügt. Der Patient starb nach einigen Monaten, doch nicht wegen der Niere, welche bis zum Tod regulär funktionierte.
Das bisherige Kronjuwel der Disziplin folgte knapp ein Jahr später: Im Januar 2025 wurde einem 66-jährigen Mann eine Schweineniere, ebenfalls von eGenesis, eingesetzt. Über ein halbes Jahr später lebt er immer noch und die Niere funktioniert regulär. Der Mann ist inzwischen 67 Jahre alt, benötigt seit acht Monaten keine Dialyse mehr und ist der bisher größte – und einzige – Beweis, dass Xenotransplantation nachhaltig funktionieren kann. Im Juni folgte ein weiterer eGenesis-Patient, ein 54-jähriger Mann, welcher seitdem offenbar ebenfalls in guter Verfassung ist und wieder arbeitet, aber noch nicht die Halbjahresmarke erreicht hat.
Große Schritte
Xenotransplantation ist offenkundig noch eine exotische Disziplin, welche mehrheitlich in der Forschungsphase und nur sanft in der Anwendung steckt. So erging es einst auch der Technologie der Transplantation im Allgemeinen. Gewissermaßen sind Xenotransplantationen heute dort, wo reguläre Transplantationen im frühen 20. Jahrhundert waren: Womöglich nur noch einige wenige parallele technologische Entwicklungen davon entfernt, einen Durchbruch zu erzielen. Genau wie das Verständnis der Abstoßungsreaktion und die Entwicklung von Immunsuppressiva in den 1960ern das gesamte Feld in eine völlig neue Bedeutung hievten.
Bereits die Durchbrüche in der Gentechnik der vergangenen Jahre haben viel bewirkt. Es ist keine Überraschung, dass sich die Erfolge der Xenotransplantation (bislang zugegebenermaßen nicht immer am Überleben ihrer Patienten gemessen) seit 2020 häufen: Erst 2012 wurde die Genschere CRISPR-Cas9 vorgestellt; einige Jahre später wurde sie dann zur Modifizierung von Schweineorganen eingesetzt. Diese Modifikation soll das Immunsystem des Patienten davon überzeugen, dass keine Abstoßung vonnöten ist – und das Risiko senken, dass sich für Schweine typische Krankheiten in den Organen ausbilden.
Die Ethik
Der Nutzen von Xenotransplantation ist recht schnell ersichtlich: Sie könnte den globalen Mangel an Spenderorganen elegant lösen und Tausende Menschenleben bewahren. Die Zahl an Schweinen, welche dafür benötigt wäre, ist im Vergleich zur globalen Züchtung für Nahrungsmittel vernachlässigbar.
Auf der anderen Seite wirft der Einsatz von Schweinen ethische Probleme auf. Vor allem religiöse Gruppen, welche negativ auf Schweine blicken oder den Körper als religiös aufgeladen werten, könnten mit Xenotransplantationen hadern. Darin wird schließlich gewissermaßen eine Chimäre aus Menschen und Schweinen kreiert, also ein Mischwesen (sowohl bei Judentum als auch Islam deutet sich jedoch bereits an, dass sie die medizinischen Vorteile stärker gewichten werden). Tierrechtsgruppen dürften die Zucht und Tötung von Tieren für die Organentnahme kritisieren. Womöglich werden die Schweine sogar am Leben gehalten und mehrfach stressvollen Operationen unterworfen.
Gut zu wissen: Bei einem Hybrid müsste jede Zelle gemischtes Erbgut beinhalten, bei einer Chimäre existieren unterschiedliche Erbgüter, ohne, dass jede Zelle betroffen sein muss. Möchte man sehr genau sein, ist jeder Mensch nach einer Bluttransfusion und ist jede schwangere Frau kurzzeitig eine Art Chimäre. Der Begriff Chimäre geht dabei auf die griechische Mythologie zurück, wo es ein Mischwesen aus Ziege, Löwe und Schlange beschreibt.
Die erhöhte Gefahr für tierische Krankheiten stellt neue Risiken für Patienten dar, welche diese allerdings in ihrer Entscheidung berücksichtigen können und die sich technologisch perspektivisch eindämmen lassen dürften. Ein exotischeres Problem wäre das Risiko der Einführung tierischer Krankheiten auf dem Populationslevel, also, dass tierische Erreger dank Xenotransplantationen nachhaltig den Sprung auf den Menschen schaffen. Großbritannien hatte deswegen schon vor 25 Jahren kurzzeitig Regeln aufgestellt, wonach sich Patienten regelmäßigen Überprüfungen stellen, ihre Adresse registrieren und beim Geschlechtsverkehr stets "Barrieremethoden" (z.B. Kondome) als Verhütungsmittel einsetzen müssen.
Näher als du denkst?
Die Xenotransplantation ist also eine junge, doch hochdynamische Disziplin, welche einen großen Nutzen für die Menschheit schaffen kann – jedoch eigene ethische Fragen aufwirft, vor allem mit Hinblick auf das Tierwohl und Krankheitsübertragungen. Diese Abwägung könnte schneller relevant werden, als manch Beobachter erwarten mag: eGenesis, welches derzeit Technologieführer zu sein scheint, hat von der US-Gesundheitsbehörde die Zulassung für eine Studie mit 33 Patienten bekommen. Schneiden sie so gut ab wie die zwei Patienten, die aktuell mit Schweineniere leben, hätte eine neue Ära begonnen.
Weiterlesen
Explainer zu Technologien
Die Zukunft der Atomenergie: Small Modular Reactors (2024)
Novo Nordisk und das Ende der Adipositas (2024)
Arm: Der wichtigste Chipdesigner der Welt (2023)
Die Zukunft der Atomenergie: Die Endlagerung (2023)
Das Ende der Atomenergie (2023)
Die Weltraumindustrie und der Staat (2022)
Die Privatisierung der Raumstationen (2021)
Die Chipindustrie und die Juwelen der Moderne (2021)
Die goldene Ära der Cyberunsicherheit (2021)
Future of Food (2021)
Explainer zu KI
Das Internet der Zukunft (2025)
Was bedeutet KI für die menschliche Intelligenz? (2025)
Wie steht es um die Adoption von KI? 2024)
Die Vergangenheit, Gegenwart und Zukunft der Künstlichen Intelligenz (2023)
Apple am entscheidenden Moment (2024)
Nvidia auf dem Gipfel (2024)

.avif)
